- Barajar
ActivarDesactivar
- Alphabetizar
ActivarDesactivar
- Frente Primero
ActivarDesactivar
- Ambos lados
ActivarDesactivar
- Leer
ActivarDesactivar
Leyendo...
Cómo estudiar sus tarjetas
Teclas de Derecha/Izquierda: Navegar entre tarjetas.tecla derechatecla izquierda
Teclas Arriba/Abajo: Colvea la carta entre frente y dorso.tecla abajotecla arriba
Tecla H: Muestra pista (3er lado).tecla h
Tecla N: Lea el texto en voz.tecla n
![]()
Boton play
![]()
Boton play
![]()
39 Cartas en este set
- Frente
- Atrás
- 3er lado (pista)
|
Propiedades de Metales
|
brillo metálico, buenos conductores de calor y electricidad, tenaces (no se deforman), maleables (placas delgadas) y dúctiles (alambres).
Todos son sólidos excepto el mercurio. |
cobre
|
|
Propiedades de los no metales
|
sin brillo, malos conductores de electricidad y calor, se encuentran en los 3 estados.
|
?
|
|
Tabla periódica
|
Es un esquema en el que se organizan y distribuyen los distintos elementos químicos conforme a sus propiedades y características, siendo su función principal establecer un orden específico agrupando sus elementos.
|
Esquema
|
|
Principales químicos organizadores de los elementos
|
Johann Wolfgang Döbereiner
Alexandre-émile béguyer de chancourtois Jonh Alexander Reina Newlands Julius Lothar Meyer Dmitri Ivanovich Mendeleiev |
lobo
verdugo newlands Meyer Mendeleiev |
|
Johann Wolfgang Döbereiner
|
En 1817 presenta un informe donde plasmaba la relación que existía entre la masa y las propiedades de diferentes elementos, comenzando así la formación de grupos de acuerdo a sus semejanzas, como las tríadas como las que se formaban cloro bromo y yodo llegando a armar alrededor de 20 tríadas.
|
trío
|
|
Alexandre-émile béguyer de chancourtois y John Alexander Reina Newlands
|
chancourtois propuso una de las formas más atractivas desde el punto de vista visual para clasificar los elementos llamada: hélice telúrica.
En 1862, Chancourtois manifiestó la periodicidad entre los elementos de la tabla. En 1864, Chancourtois y Newlands, anunciaron la ley de las octavas la cual nos manejaba que las propiedades se repiten cada 8 elementos. pero este método se dejaba de cumplir en los elementos más allá del calcio, por lo que esta clasificación es insuficiente. |
Periodicidad, ley de octavas
|
|
julius lothar Meyer
|
este químico identifica una serialización de las propiedades físicas de los elementos que se basa en el volumen y número atómico, punto de fusión y ebullición, entre otras propiedades.
Meyer trabajo en diversas áreas de la química pero su mayor esfuerzo se centra en la preocupación de clasificar los elementos químicos y en adopción de sus propiedades químicas para predecir su comportamiento periódico en la tabla. |
Propiedades físicas de los elementos
|
|
Dimitri ivánovich mendeleiev
|
En 1869, mendeleiev presentó una nueva versión de su tabla periódica, esta tabla fue la primera presentación coherente de las semejanzas de los elementos se dio cuenta de que el clasificar los elementos según sus masas atómicas se veían aparecer una periodicidad en lo que concierne a ciertas propiedades de los elementos la tabla en ese entonces tenía 63 elementos.
|
Masas atómicas
|
|
Tabla periódica actual
|
La tabla periódica actual se encuentra estructurada con base en el número atómico creciente de los elementos. Las columnas verticales de la tabla periódica se conocen como grupos o también llamados familias y el que incluyen elementos con idéntica Valencia atómica y características para reaccionar semejantes presentando por lo tanto propiedades parecidas entre sí.
los periodos son las filas horizontales que inician con un elemento metálico y finalizan con un gas noble agrupa los elementos con propiedades que son diferentes pero cuyas masas resultan similares estos elementos difieren en propiedades pero tienen la misma cantidad de niveles energéticos o de electrones. Cada nivel de arriba para abajo es un nivel más de electrones en su estructura atómica. |
Periodos, grupos o familias, nivel de electrones
|
|
tabla periódica larga
|
La tabla periódica actual se le llama larga considerando los descubrimientos de los elementos que se han hecho actualmente. Los grupos son enumerados con números romanos.
|
Romanos
|
|
periodos
|
los elementos se distribuyen en filas horizontales llamadas periodos los periodos no son todos iguales sino que el número de elementos que contiene va cambiando aumentando al bajar en la tabla periódica el período determina el número de niveles energéticos que tiene un átomo es decir si un átomo tiene 5 niveles energéticos entonces su número de periodos será igual 5.
|
niveles energéticos
|
|
bloques
|
la tabla periódica se puede también dividir en bloques de los elementos según el orbital en que están ocupados los electrones más externos los bloques se le denominan según la letra que hace referencia entonces tenemos que los bloques se designan según su configuración electrónica.
|
s, p, d, f
|
|
configuración electrónica
|
la configuración electrónica se muestra en el ordenamiento de los electrones de cada elemento.
1 s, 2s 2p 3s 3p 4S 3D 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d y 7d. |
diagonales
|
|
Electrones de Valencia
|
seda a base de la última letra s y la letra p
a excepción de que terminen en d f allí sólo se tomará la última letra s. |
s + p?
|
|
configuración de kernel
|
se basa en lo último de la configuración electrónica. se saca de acuerdo a los bloques. y de arriba hacia abajo va creciendo. de arriba hacia abajo sería 1s 2s 3s 4s 5s 6s 7s. y de izquierda a derecha sería s1 s2 d1 d2 d3 d4 d5 d6 d7 d8 d9 d10 p1 p2 p3 p4 p5 p6. y de arriba hacia abajo se va agregando más renglones de acuerdo al bloque en el que pertenecen al período.
|

|
|
propiedades periódicas
|
carácter metálico, radio atómico, volumen atómico, radio iónico, energía de ionización, electroafinidad y electronegatividad, poder oxidante y poder reductor
|
Metal 1
átomo 2 ion 2 + - oxidar y reducir |
|
propiedades periódicas (qué son)
|
son características propias de los elementos que varían según su número atómico
|
características, número
|
|
carácter metálico
|
un elemento se considera metal desde un punto de vista electrónico cuando cede fácilmente sus electrones y no tiene tendencia a ganarlos es decir los metales son muy poco electronegativos un no metal es todo elemento que difícilmente cede.
|
de derecha a izquierda y de arriba hacia abajo. francio+ y flúor-
|
|
radio atómico
|
el radio atómico es la mitad de la distancia entre dos núcleos de átomos adyacentes unidos por un enlace covalente.
|
de arriba a abajo, de derecha a izquierda
|
|
volumen atómico
|
el volumen atómico es el volumen que ocupa un mol de un átomo del elemento considerado y se obtiene según la ecuación masa del átomo entre densidad. se tiene que considerar en caso de que sea gaseoso la densidad del líquido, en sólidos con estructuras alotrópicas el más estable, en sólidos con estructura cristalina alotrópica el número de coordinación.
|
de arriba hacia abajo, de derecha a izquierda
|
|
radio iónico
|
hace referencia al radio que presenta un átomo que ha ganado o perdido electrones.
un ion positivo tiene un radio iónico menor al radio atómico de un elemento neutro. un ion negativo tiene un radio iónico mayor al radio atómico del elemento neutro. el radio atómico será tanto menor cuanto mayor sea la carga positiva del ion y tanto mayor cuanto sea la carga negativa. |
de arriba hacia abajo de derecha a izquierda
|
|
energía de ionización
|
es la energía mínima requerida para separar un electrón de un átomo o molécula específica a una distancia tal que no existe interacción electrostática entre el ión y el electrón
|
de abajo hacia arriba de izquierda a derecha.
|
|
poder oxidante
|
un oxidante es una especie química que produce oxidación de otra. gana electrones
|
de abajo hacia arriba de izquierda a derecha
|
|
poder reductor
|
tiene la capacidad de ceder electrones al oxidante. Pierde electrones.
|
de arriba hacia abajo de derecha a izquierda.
|
|
electroafinidad
|
la capacidad que tiene un elemento para poder captar electrones Por ende los metales serán los que tengan una electroafinidad menor.
|
de arriba hacia abajo de izquierda a derecha
|
|
electronegatividad
|
capacidad que tiene un elemento para atraer electrones o densidad electrónica cuando forma un enlace.
|
de abajo hacia arriba de izquierda a derecha.
|
|
tipos de enlace
|
iónico, covalente polar y no polar, metálico
|
4
|
|
regla del octeto
|
la regla del octeto fue anunciada en 1916 Por Gilbert Lewis y Walter kossel de manera independiente. esta regla nos maneja que los átomos de los elementos se unen los unos a los otros en el intento de completar su capa de Valencia para lograr estabilidad sugerida por la regla del octeto cada elemento necesita ganar o perder electrones en los enlaces químicos y así conseguir ocho electrones en la capa de Valencia.
|
Enlaces con 8 electrones
|
|
estructura de Lewis
|
en este esquema se usan puntos y x para generar un enlace de manera que se completen los ocho electrones de valencia.
|
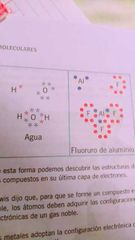
|
|
enlace iónico
|
en este enlace los electrones de un elemento son sustraídos y se incorporan a otro quedado con deficiencia de electrones y por lo tanto con carga positiva y el elemento receptor de los electrones tendrá exceso de carga eléctrica por lo tanto estará con carga negativa.
|
positivo y negativo.
metal y no metal |
|
enlace covalente
|
en este tipo de enlace se forma cuando los electrones de la última capa se comparte es decir no hay desprendimiento de esto.
|
neutral (como ley de octetos (?)) entre no metales.
|
|
enlace covalente polar.
|
este se forma cuando la molécula no es simétrica por lo cual se originan polos de carga eléctrica el agua es un ejemplo de esto.
|
no simétrico
|
|
enlace covalente no polar
|
en este enlace hay simetría y no hay polos.
|
simétrico
|
|
fuerzas intermoleculares
|
las fuerzas intermoleculares son aquellas de atracción entre moléculas que ejercen más influencia sobre los sólidos y los líquidos.
allí tenemos las fuerzas dipolo-dipolo las fuerzas de London y las del enlace por Puente de hidrógeno. |
sólido y líquido
|
|
enlace metálico
|
se describe como una nube de electrones alrededor de núcleos x distantes en esta novela Vega los electrones libremente formando un enlace resistente que repele la luz.
|
metales
|
|
dipolos inducidos o fuerzas dipolo-dipolo
|
denominados dipolos a las moléculas que disponen de zonas cargadas negativamente y positivamente debido a la electronegatividad y concentración de los electrones en las moléculas.
|
positivo y negativo.
|
|
fuerzas de London
|
las fuerzas de dispersión de London denominadas así en honor al físico germano fritz London son fuerzas intermoleculares débiles que surgen de fuerzas interactivas entre multipolos temporales en moléculas y momento multipolo permanente.
|
grandes
|
|
enlace por Puente de hidrógeno
|
la formación de puentes de hidrógenos es determinante en la configuración espacial de las macromoléculas que constituyen los sistemas biológicos como proteínas y ácidos nucleicos así como la formación y estabilización de asociaciones complejas entre macromoléculas como sucede con los lípidos y proteínas en las membranas celulares.
|
ADN, agua
|
|
Diferencia entre los enlaces
|
Menor o igual a 0.4 - Covalente no polar
De 0.5 a 1.7 - Covalente polar Mayor a 1.7 - Iónico |
0.4 - 1.7
|