- Barajar
ActivarDesactivar
- Alphabetizar
ActivarDesactivar
- Frente Primero
ActivarDesactivar
- Ambos lados
ActivarDesactivar
- Leer
ActivarDesactivar
Leyendo...
Cómo estudiar sus tarjetas
Teclas de Derecha/Izquierda: Navegar entre tarjetas.tecla derechatecla izquierda
Teclas Arriba/Abajo: Colvea la carta entre frente y dorso.tecla abajotecla arriba
Tecla H: Muestra pista (3er lado).tecla h
Tecla N: Lea el texto en voz.tecla n
![]()
Boton play
![]()
Boton play
![]()
44 Cartas en este set
- Frente
- Atrás
- 3er lado (pista)
|
¿Cuál es el significado etimologico del átomo?
|
es partícula indivisible
|
|
|
¿Dónde nace el concepto del átomo y por quién?
|

Su concepto nace en Grecia y es
obra del filósofo y matemático Demócrito. |
|
|
¿Quienes sentaron las bases de los postulados científicos respecto del átomo durante el periodo de la ilustración?
|
Durante el periodo de la Ilustración,
Lavoisier, Dalton y Avogadro sentaron las bases para el conjunto de postulados científicos respecto del átomo. |
|
|
¿En qué año y quién construye el primer modelo atómico?
|

En 1803, Dalton construye el primer
modelo atómico con bases científicas. |
|
|
¿Cuáles son las tres partículas subatómicas?
|
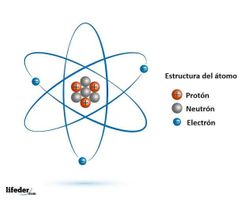
Electrones, protones, Neutrones
|
|
|
¿Por quien fueron descubiertos los electrones y en qué año ?
|
Descubiertos por J. J. Thompson
en 1897. |

|
|
¿De que son responsables los electrones?
|
Responsables de los procesos de
combinación entre átomos y por tanto entre elementos químicos. |
|
|
¿Que tipo de carga tienen los electrones?
|
Carga negativa
|
|
|
¿Cómo es la masa de los electrones?
|
Partículas de menor masa en el
átomo. La masa es tan pequeña que es discriminada en el conteo de masa total del átomo. |
|
|
¿Cómo están representados los electrones en el modeló atómico de Bohr?
|
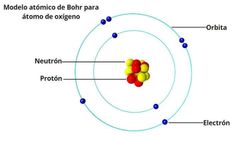
Los electrones se encuentran en
movimiento en la parte más externa del átomo en órbitas definidas |
|
|
¿Cómo se encuentran los electrones en el modeló atómico actual?
|
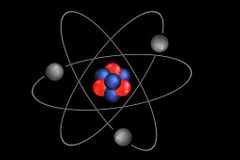
Los electrones no tienen órbitas
definidas y los espacios en los que se distribuyen corresponden a subniveles energéticos. |
|
|
¿Que es la configuración energética?
|
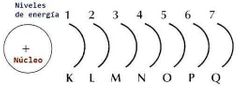
A la secuencia de subniveles
energéticos en los que se organizan los electrones de un átomo se le conoce como Configuración Electrónicas |
|
|
¿En dónde se encuentran los protones?
|
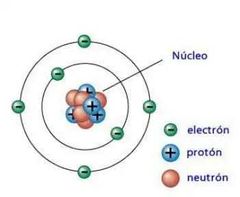
Se encuentran en el núcleo
atómico. |
|
|
¿Que carga tienen los protones?
|
Poseen carga positiva de igual
magnitud a la del electrón. |
|
|
¿Cómo es la masa de los protones?
|
Su masa es considerada la unidad
de la masa del átomo: 1uma. |
|
|
¿Que representa la cantidad de protones?
|
la identidad del átomo
|
|
|
¿Que carga tienen los neutrones?
|
carecen de carga eléctrica
|
|
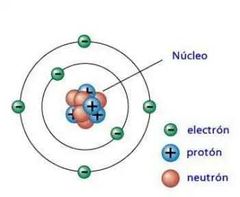
¿Es relevante el neutrón para determinar la identidad del átomo?
|
No es relevante para determinar la
identidad del átomo pero su número puede variar en los átomos de un mismo elemento y a estas formas se les conoce como isótopos. |
|
|
¿Que características tenía el modelo atómico de Rutherford?
|
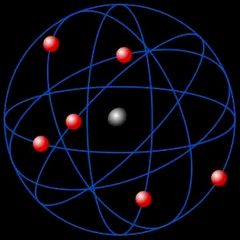
Núcleo definido
Protones con carga positiva dentro del núcleo Electrones alrededor del núcleo |
|
|
¿por dónde se transmite la Luz?
|
por ondas
|
|
|
¿Que es la longitud de onda?
|
distancia entre cresta y cresta
|
|
|
¿Que es la frecuencia de onda?
|
Cantidad de ondas por unidad de tiempo
|
|
|
¿cuáles son las medidas en que la Luz es visible en el espectro?
|
400nm a 700nm
|
|
|
¿Que dice la teoría cuántica de Planck?
|
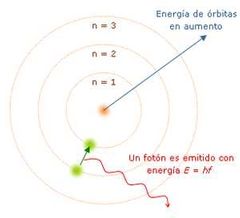
A valores específicos de luz
incidente, los metales pueden liberar electrones La materia absorbe o emite energía en paquetes conocidos como cuantos |
|
|
¿Cómo Einstein consideraba a la luz?
|
Einstein considera a la luz como
un torrente de partículas llamadas fotones (Dualidad onda/partícula) |
|
|
¿Cómo consideraba el modelo atómico de borh a los electrones?
|
que los electrones están cuantizados
|
|
|
¿Cómo determina Borh las distancias de los electrones al núcleo?
|
Determina distancias de los
electrones al núcleo dependiendo de la energía que los electrones poseen |
|
|
¿Cuantos niveles energéticos existen?
|
7 niveles con distinta capacidad
de albergar electrones |
|
|
¿Cuáles son estos 7 niveles energéticos?
|
2
8 18 32 32 18 8 |
|
|
¿Cómo era el modelo atómico de Borh?
|
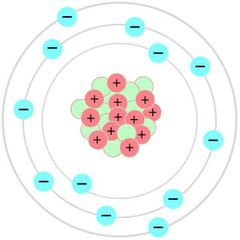
Representación de un elemento
y los electrones que posee distribuidos en orbitales |
|
|
¿Cómo se organiza la tabla periódica?
|

Familias y periodos
|
|
|
¿Que son las familias?
|

Conjuntos verticales de la tabla
periódica que agrupan elementos con reactividades semejantes por lo que comparten la valencia. |
|
|
¿Que son los periodos en la tabla periódica?
|
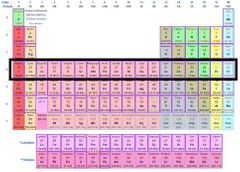
Conjuntos horizontales de la tabla
periódica en la que los elementos comparten el último nivel energético de sus átomos |
|
|
¿Cómo se expresa el número atómico?
|

Se le express cómo la letras mayúscula Z
|
|
|
¿Cómo se calcula el número atómico?
|
Se calcula con el conteo de
protones en el núcleo atómico. |
|
|
¿Que tipo de valor es el número atómico?
|
El número atómico es el valor que
organiza la secuencia de elementos en la tabla periódica. |
|
|
¿Cómo se puede indentificar el número atómico en la tabla periódica?
|
En la tabla periódica se puede
identificar como un número entero. |
|
|
¿Que es la masa atómica?
|
Cantidad de masa presente en el
átomo. |
|
|
¿Cómo se calcula la masa atómica?
|
Se calcula como la suma del
número de protones y neutrones del átomo. |
|
|
¿Cómo se identifica la masa atómica en la tabla periódica?
|

Se identifica en la tabla periódica
como un número con decimales pues considera la proporción de todos los isótopos existentes de un elemento |
|
|
¿Que es la Valencia?
|

Número de electrones que un
átomo tiene en su último nivel energético. |
|
|
¿Cómo se identifica y se agrupan los elementos que comparten Valencia?
|
En la tabla periódica, los elementos
que comparten valencia se agrupan de manera vertical en familias. |
|
|
¿Que es el número de oxidación?
|

Los electrones que un átomo gana
o pierde en los procesos de reacción química. |
|
|
¿Cómo identificamos la identidad de una sustancia o que tipo de elemento pertenece a el átomo?
|
al número de protones
|