- Barajar
ActivarDesactivar
- Alphabetizar
ActivarDesactivar
- Frente Primero
ActivarDesactivar
- Ambos lados
ActivarDesactivar
- Leer
ActivarDesactivar
Leyendo...
Cómo estudiar sus tarjetas
Teclas de Derecha/Izquierda: Navegar entre tarjetas.tecla derechatecla izquierda
Teclas Arriba/Abajo: Colvea la carta entre frente y dorso.tecla abajotecla arriba
Tecla H: Muestra pista (3er lado).tecla h
Tecla N: Lea el texto en voz.tecla n
![]()
Boton play
![]()
Boton play
![]()
6 Cartas en este set
- Frente
- Atrás
- 3er lado (pista)
|
Litio
|
Se evapora la solución con Li+ dejando una solucion concentrada. Se le agrega Carbonato (CaO3), formando Li2CaO3.
Precipita y se exporta o se vuelve a purificar. |
|
|
Sodio (Na)
|
Obtencion: Celda Down 800°C
-NaCl se mezcla con CaCl2 para bajar el punto de fusión (600°C). -Se calienta -Entra a la celda Down. -En el anodo se forma Cl2 -Catodo de hierro, se reduce el sodio -Cl2 se evapora. -Enfriar Ca y Na -Ca queda solido y Na liquido. -Na sale como producto. |
Celda Down
|
|
Potasio
|
-Fundir KCl y Na generando una Redox donde Na se oxida y K se reduce.
KCl + Na →K + NaCl |
|
|
Bateria Litio
|
El Litio metalico se oxida a Li+ y el Oxido de Magnesio se reduce.
El material poroso se impregna de un electrolito organico para conducir la electricidad. |
|
|
Bateria Ion litio.
|
-Capacidad del Litio de incrustarse en una red cristalina.
-Los iones de litio estan encajados en capas del oxido mixto (LiCoO2 Ánodo) -Al aplicar una diferencia de potencial adecuada es posible moverlos, estos son atraidos al electrodo grafito (cátodo). Este es el proceso de carga. -En la descarga, los cationes de Li+ vuelven a su posición original |
Hexagonos y Triángulos
|
|
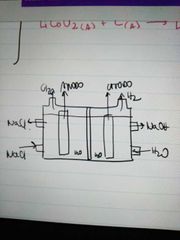
Bateria Hidroxido de sodio
|
-Electrolisis de solución acuosa de NaCl que produce H2 y Cl2 gas ademas de NaOH.
-Separados por una membrana para no formar HCl 2H2O (l) +2NaCl(ac)→Cl2(g) +H2(g)+NaOH(ac) |
|