- Barajar
ActivarDesactivar
- Alphabetizar
ActivarDesactivar
- Frente Primero
ActivarDesactivar
- Ambos lados
ActivarDesactivar
- Leer
ActivarDesactivar
Leyendo...
Cómo estudiar sus tarjetas
Teclas de Derecha/Izquierda: Navegar entre tarjetas.tecla derechatecla izquierda
Teclas Arriba/Abajo: Colvea la carta entre frente y dorso.tecla abajotecla arriba
Tecla H: Muestra pista (3er lado).tecla h
Tecla N: Lea el texto en voz.tecla n
![]()
Boton play
![]()
Boton play
![]()
15 Cartas en este set
- Frente
- Atrás
|
Tabla Periódica
|
El arreglo de elementos en orden creciente de su número atómico, dónde los elementos con propiedades similares se encuentran en columnas verticales se llama tabla periódica.
|
|
Historia de la Tabla Periódica.
|
A principios del siglo XXI, a medida que crecía la lista de elementos conocidos, se intentaba descubrir patrones en el comportamiento químico. Esos esfuerzos culminaron en 1869, cuando se desarrolló la tabla periódica.
|
|
Diseño de la tabla periódica
|
Fue diseñada por el químico ruso Dmitri Mendeleev en 1899, es un cuadro que representa todos los elementos químicos que existen, ordenados según sus propiedades físicas.
|
|
Elementos Químicos
|

Para cada elemento, la tabla indica el número y símbolo atómicos, y con frecuencia también se da la masa atómica.
|
|
Ley de la Periodica de Mendeleev
|
Mendeleev propuso la ley periódica en la que postuló que las propiedades de los elementos químicos dependen periódicamente de sus pesos atómicos.
|
|
Ley periódica y periodicidad de Mendeleev
|
Postula que las propiedades químicas y físicas dependen del número atómico.
|
|
Ley periódica moderna de Moseley
|
La ley de Moseley es una ley empírica que establece una relación sistemática entre las longitud de onda de los rayos x emitidos por distintos átomos con su número atómico
|
|
Ley periódica moderna de Moseley
|
Establece que las propiedades físicas y químicas de los elementos químicos tienden a repetirse de forma sistemática conforme aumenta el número atómico.
|
|
Ordenamiento de los Elementos en la tabla periódica:
|
-Las filas horizontales se conocen como periodos.
-Las columnas (verticales) son grupos, clasificados en tres esquemas, separados en elementos metálicos, metálicos y metaloides. |
|
Periodos y Columnas:
|
Actualmente, la tabla periódica se compone de 118 elementos distribuidos en 7 filas horizontales llamadas períodos y 18 columnas verticales, conocidas como grupos.
|
|
Fórmulas Alcalinas:
|
Los metales alcalinos, junto con el Hidrógeno (que es un gas) constituyen el grupo 1 que se encuentra en el bloque- s de la tabla periódica.
|
|
Metales Alcalinotérreos:
|
Conforman la familia IIA de elementos, se encuentran situados en el grupo 2 de la tabla periódica. (Be, Mg, Ca, Sr, Ba, Ra).
|
|
Fórmula de los Halógenos:
|
La fórmula de los Halógenos es R-X dónde X puede ser cualquier Halógeno: -F, -Cl, -Br, -I.
|
|
Fórmulas de las leyes de los gases:
|
-Ley de Boyle. P=kV//P1.V1=P2.V2
-Ley de Charles. V=k.T//V1T1=V2T2 -Ley de Gay-Lussac. P=k.T//P1T1=P2T2 -Ley de los Gases. P.V=k.T//P.V=n.R.T |
|
Diferencias Periódicas entre las fórmulas de la Tabla Periódica:
|
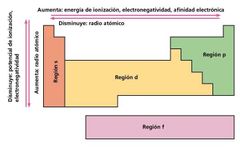
Dependen de su número atómico. Se ubican por número atómico creciente y las propiedades que presentan de relacionan con ese número, es posible predecir sus propiedades físicas y químicas así como su comportamiento químico.
|