- Barajar
ActivarDesactivar
- Alphabetizar
ActivarDesactivar
- Frente Primero
ActivarDesactivar
- Ambos lados
ActivarDesactivar
- Leer
ActivarDesactivar
Leyendo...
Cómo estudiar sus tarjetas
Teclas de Derecha/Izquierda: Navegar entre tarjetas.tecla derechatecla izquierda
Teclas Arriba/Abajo: Colvea la carta entre frente y dorso.tecla abajotecla arriba
Tecla H: Muestra pista (3er lado).tecla h
Tecla N: Lea el texto en voz.tecla n
![]()
Boton play
![]()
Boton play
![]()
3 Cartas en este set
- Frente
- Atrás
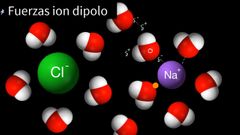
Responsable de la interacción entre los iones y otra sustancia polar. Un ejemplo sencillo es la disolución de un sólido iónico, o sal, en agua. Cuando la sal de mesa (NaCl) se disuelve en agua, las interacciones entre los iones y las moléculas de agua son lo suficientemente fuertes como para superar el enlace iónico que retiene los iones en la red cristalina. Como resultado, los cationes y aniones se separan completamente, y cada ion está rodeado por un cúmulo de moléculas de agua. Esto se llama un proceso de solvatación. La solvatación ocurre a través de la fuerte fuerza ión-dipolo. Las sales de lotes, o compuestos iónicos, son solubles en agua debido a tales interacciones.
|
Las fuerzas dipolo-dipolo se dan entre moléculas con dipolos permanentes (es decir, moléculas polares).
Un ejemplo de fuerza dipolo-dipolo lo tenemos entre moléculas de cloroformo. |
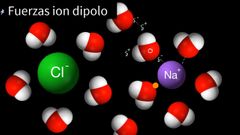
El resultado de las interacciones coulombianas entre dipolos instantáneos.
Se presentan en moleculas no-polares, a traves de la formación de dipolos inducidos en moleculas adyacentes |
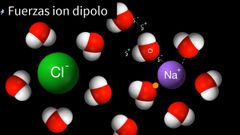
se presentan en moleculas no-polares, a traves de la formación de dipolos inducidos en moleculas adyacentes
|
|
se presentan en moleculas no-polares, a traves de la formación de dipolos inducidos en moleculas adyacentes
|
se presentan en moleculas no-polares, a traves de la formación de dipolos inducidos en moleculas adyacentes
|