- Barajar
ActivarDesactivar
- Alphabetizar
ActivarDesactivar
- Frente Primero
ActivarDesactivar
- Ambos lados
ActivarDesactivar
- Leer
ActivarDesactivar
Leyendo...
Cómo estudiar sus tarjetas
Teclas de Derecha/Izquierda: Navegar entre tarjetas.tecla derechatecla izquierda
Teclas Arriba/Abajo: Colvea la carta entre frente y dorso.tecla abajotecla arriba
Tecla H: Muestra pista (3er lado).tecla h
Tecla N: Lea el texto en voz.tecla n
![]()
Boton play
![]()
Boton play
![]()
10 Cartas en este set
- Frente
- Atrás
|
Ecuación de Schrodinger
|
Se obtiene funciones de onda: obtener orbitales y energía de los electrones.
|
|
Números cuánticos
|
1. Principal o energético (n)
2. Secundario o azimutal (l) 3. Magnético (m) 4. Espin (s) |
|
número cuántico (n)
|
-Indica energía de los orbitales
-Cuarto más pequeño al número, más cerca del núcleo |
|
número cuántico (l)
|
-Indica forma de los orbitales
-depende de n órbita> s p d f valor l> 0 1 2 3 |
|
número cuántico (m)
|
-Indica la orientación espacial de los orbitales
orbital s= 0 orbital p= -1, 0, 1 orbital d= -2, -1, 0, 1, 2 orbital f= -3, -2, -1, 0, 1, 2, 3 |
|
número cuántico (s)
|
-Indica el sentido de la rotación
-Independiete - +1/2 ó -1/2 ↑. ↑↓ Desapareado (espines paralelos) Apareado (espines antiparalelos) |
|
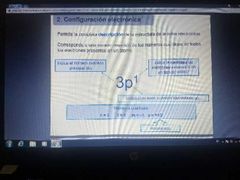
Configuración electrónica
|
Descripción de la estructura de la nube electrónica
|
|
Principio de exclusión de Pauli
|
Si se quiere colocar más de un electrón en un mismo orbital, cambia el número cuántico (s)
|
|
Principio de Aufbau
|
Los e- ocupan los orbitales de menor energía, y progresivamente se van llenando los orbitales de mayor energía.
|
|
Regla de máxima multiplicidad de Hund
|
Las partículas subatómicas son más estables cuando presentan electrones desapareados que cuando están apareados.
|