- Barajar
ActivarDesactivar
- Alphabetizar
ActivarDesactivar
- Frente Primero
ActivarDesactivar
- Ambos lados
ActivarDesactivar
- Leer
ActivarDesactivar
Leyendo...
Cómo estudiar sus tarjetas
Teclas de Derecha/Izquierda: Navegar entre tarjetas.tecla derechatecla izquierda
Teclas Arriba/Abajo: Colvea la carta entre frente y dorso.tecla abajotecla arriba
Tecla H: Muestra pista (3er lado).tecla h
Tecla N: Lea el texto en voz.tecla n
![]()
Boton play
![]()
Boton play
![]()
135 Cartas en este set
- Frente
- Atrás

|
H2SO4 caliente
(con carbonos primarios y segundarios porque puede haber eliminación con 3°) |

|

|

|
R'-Cl
primarios y secundarios porque es SN2 (en halogenos 3° puede haber reaccion de competencia) |

|
HX
dónde X es un halogenuro, se formarán en mayor cantidad los más estables |
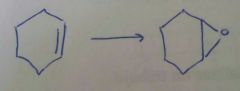
|
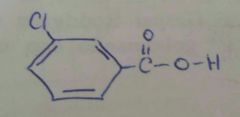
MCPBA
(acido meta cloro peroxibenzoico) |
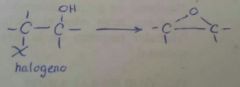
|
base fuerte
|
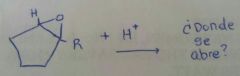
|
Siempre formará el carbocation más estable
|
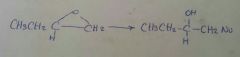
|
El Nucléofilo entra donde hay menos impedimento, el H proviene del medio acido
|

|
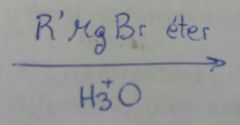
|
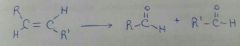
|
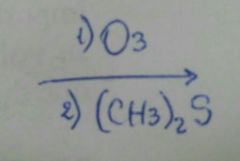
|
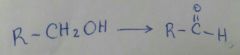
|
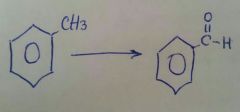
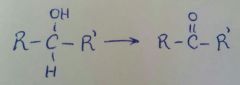
PCC
(Cloro cromáto en piridina) |

|
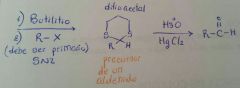
|
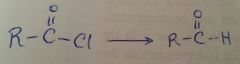
|
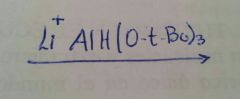
Hidruro de triterbutoxi aluminio litio
|
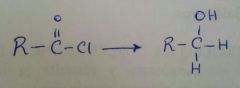
|
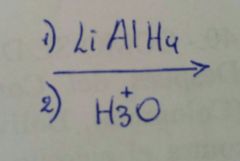
|
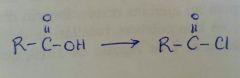
|
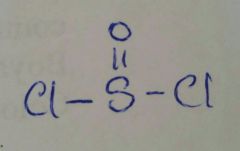
Cloruro de tionilo
(produce el cloruro de ácido y HCL SO2 gaseosos) |
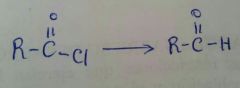
|
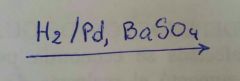
Reducción de Rosenmund
(se produce el aldehido y HCl) |
|
|
|
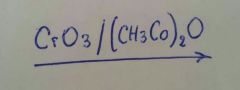
|
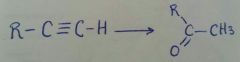
|
|
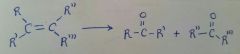
|
|
|
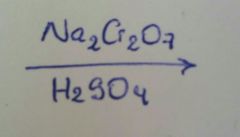
|
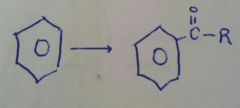
|
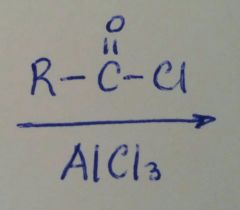
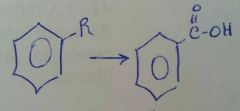
Acilacion de Friedel Crafts
|
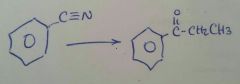
|
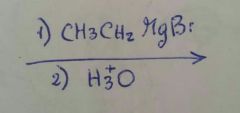
|
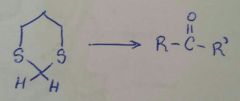
|
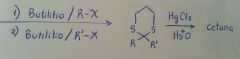
|

|

|

|

|

|
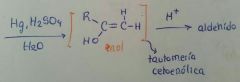
H2O
Puede mantenerse como gem-diol si existe un grupo que le quite densidad electrónica en R o en R' |

Explicar el mecanismo en medio ácido
|
Al finalizar el mecanismo de obtiene el mismo producto y se libera H+
|

Explicar el mecanismo en medio básico
|
Al finalizar el mecanismo se obtiene el mismo producto y se libera OH-
|

|
R'OH
|

|
R''OH
Si el reactivo inicial es un aldehido se producen acetales |

|
R''OH
|

|
R'''OH
Si el reactivo inicial es una cetona se producen cetales |

|
R''OH en medio ácido
(si se quiere hemicetales se lo hace una vez, si se quiere cetales se lo hace dos veces) |

|
R''OH en medio básico
(no hay cetales porque en la segunda parte el OH es mal grupo saliente) |

|

Primero se protege formando un cetal con un alcohol (en este caso CH3CH2OH) en medio ácido
|

cianohidrina alfa hidroxinitrilo
|

|

|
H+
(ácido) libera H2O |

|
H3O+
|

|
NH3
|

|
H3O+
|

|

|

|

Se usan compuestos de órganolitio porque la molecula con el grupo carbonilo tiene impedimento estérico.
El Li es mas pequeño que el Mg por eso no es recomendable usar grignard |

|

Se obtiene por adición-eliminación
|

|

Se obtiene por adición-eliminación
|
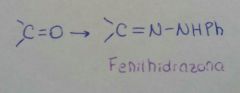
|
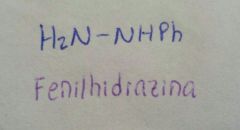
Se obtiene por adición-eliminación
con trazas de H2SO4 |

|

Se obtiene por adición-eliminación
|

|
Se agrega H+ para formar un carbocation en el carbonilo y se añade una amina primaria
(hay adición eliminación ) |

|
Se agrega H+ para formar un carbocation en el carbonilo y se añade una amina secundaria
(se libera un H para formar el doble enlace) |

|

no debe mezclarse con agua porque el Al forma hidroxidos
|

|

|

|

|

|

|

|

|

|

|

|

reduccion de Wolf kishner
|

|

|

|

Reaccion de cannizaro
(condensacion) |
|
las aminas ¿cuándo donan protones? y ¿cuando donan electrones?
|
Aminas terciarias: donan electrones
Aminas primarias: donan protones |

|

la amina actúa como base
(el I es buen grupo saliente) |

|
HX (donde H es ácido y X es halogeno)
La amina actúa como base |

|

|

|

Se forma anilina, NaCl y H2O
|

|

Se forma anilina y se libera HCl gas
|

|

Se puede formar aminas primarias, secundarias y terciarias.
Se detiene la reacción con NaOH |

|

La amina actúa como Nucléofilo
|

|
NaOH
(se produce NaX y H2O) |

|

|

|
NH3
|

|
Se calienta
(da el producto y también forma agua) |

|
NH3 en exceso
se forma la sal de amonio y la amina segundaria o terciaria (si se repite el proceso varias veces). Se puede usar NaOH para detener la reacción si se desea |

|
Sn (granulado) /HCl
|

|

|

|

|

|

|

|

Reordenamiento de Hoffman
(se produce CO2, H2O y 2Br-) |

|

|

|

|

|

|

|

libera HCL
Cuando es una amina terciaria no hay reaccion porque no se liberará HCl |

|

HNO2
(se usa NaNO2 y H2SO4 en frío para formarlo) |

|

|

|

|

|

|
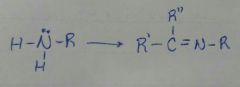
|
Solo ocurre con aminas primarias o amoniaco
Se agrega un aldehido o cetona con trazas de acido, en el proceso se libera agua y H+ para formar el doble enlace |

|
HONO
|
|
¿Cómo se puede formar aminas con alto peso molecular?
|
NH3 + RX ; dónde X es un halogeno
para agregar más grupos a la amina formada debe existir NH3 en exceso. se detiene con una base |

|
NaNO2 + 2HCl
|

|
Calor
se produce agua tambien |

|

|

|

|

|
con H3O+
También se produce NH4 |

|

con CO
|

|

se produce LiOH también
|

|

formacion de enaminas
Reacciona un aldehido o cetona con una amina segundaria. Debe haber hidrógeno para que se forme agua y salga. Al final de la reacción se libera un H+ para formar el doble enlace |

|
+ AgO
se produce AgX (insoluble) |

|
CO2
|

|
OH-
(base fuerte) |

|
NaOH
Formación de sales |

|

(para formar aspirina se sigue la reacción de kolbe)
|

|
H3O+
|

|
NH3
|
|
¿Porqué se llaman derivados de acido carboxilico?
|
Porque provienen del acido carboxilico.
Ademas se considera otros "derivados" si por medio de hidrólisis permiten obtener acido carboxilico |

|
HI
(el yodo es el menos electronegativo de los halogenos y tiene radio grande) |

|

dos veces
|

|

1. se forma una sal
2. hay una hidrolisis y el acido carboxilico se regenera |

|
2NH3
|

|

el producto formado es un compuesto carbonilico alfa-beta no saturado
|

|
Calor
(se produce CO2) |

|
calor
(se produce CO2) |
|
Explique la reacción de sustitución nucleofilica
|

- Se da en derivados de acido carboxilico
- L debe ser un buen grupo saliente - En aldehidos y cetonas hay adición nucleofilica porque tienen malos grupos salientes |
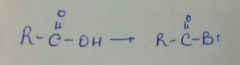
|
PBr3
|
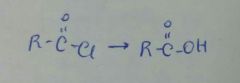
|
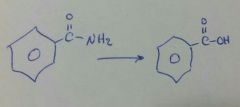
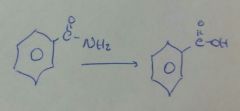
H2O
|
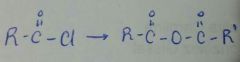
|
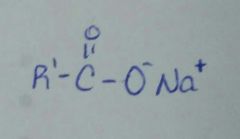
|
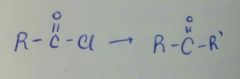
|
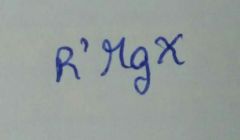
|
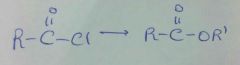
|
HOR'
|
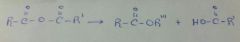
|
HOR'''
|
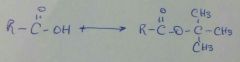
|
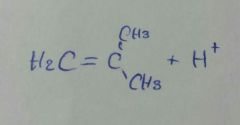
|
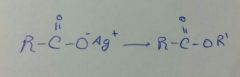
|
R'X
(X=halogeno) SN2 |
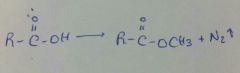
|
CH2N2 /Et2O
|
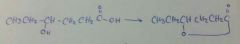
|
H+
formación de lactonas |
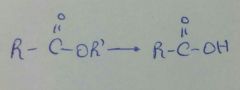
|
H3O+
|
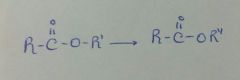
|
HOR" / catalizador
(cat= minerales, alcoholatos o en medios alcalinos) |
|
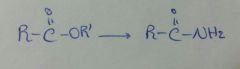
NH3
Amonolisis |
|
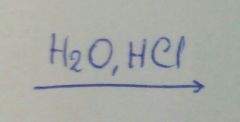
|
|
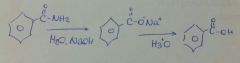
|
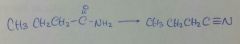
|
POCl3 / -H2O
|
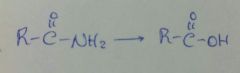
|
HNO2
(se libera H2O y N2) |
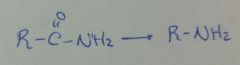
|
NaBrO
|

|
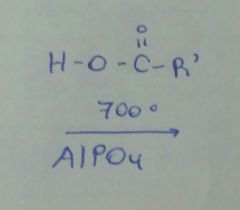
|
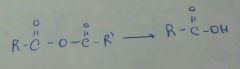
|
H2O
|
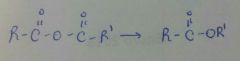
|
ROH
|
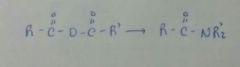
|
HNR'2
|
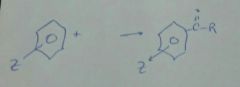
|
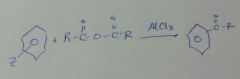
AlCl3 sirve de catalizador
|
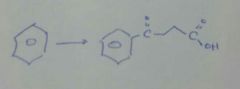
|
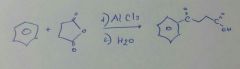
el H2O rompe el complejo
|